fusion
![Diagramme de phases [4] Diagramme de phases [4]](/encyclopedie/data/vignettes/1003577-Diagramme_de_phases_4.jpg)
Passage d'un corps de l'état solide à l'état liquide ; état d'un corps liquéfié.
THERMODYNAMIQUE
1. Le point de fusion
Lorsqu'on fournit à pression constante de la chaleur à un solide pur, sa température s'élève, puis, lorsqu'il a atteint une certaine température, appelée point de fusion, la température reste constante et du liquide apparaît. La température reste constante tant que le solide et le liquide coexistent ; lorsque tout le corps est fondu, la température s'élève à nouveau.
2. Chaleur latente de fusion
Ainsi, le point de fusion désigne la température précise où un corps pur commence à passer de l'état solide à l'état liquide, température qu'il conserve à pression constante tant que la fusion n'est pas terminée.
![Diagramme de phases [4] Diagramme de phases [4]](/encyclopedie/data/images/1003577-Diagramme_de_phases_4.jpg)
Pendant la fusion, toute la chaleur fournie au corps sert à la transition de phase ; c'est la chaleur latente de fusion, qui est toujours positive. Il faut noter que tout cela n'est pas vrai dans le cas des corps amorphes, pour lesquels le passage à l'état liquide s'effectue avec variation de la température : c'est la fusion pâteuse des verres.
La fusion est une transition de phase du premier ordre ; la chaleur latente de fusion L est donnée par la formule de Clapeyron :
dP/dT = L/T(v1 – v2)
où v1 et v2 sont les volumes molaires du corps dans les deux phases considérées.
3. Changements de volume

Le volume de la plupart des corps augmente lors de la fusion, mais ce n'est pas le cas de l'eau, par exemple. La température de fusion dépend de la pression, mais beaucoup moins que celle d'ébullition. Pour les corps dont le volume augmente lors de la fusion, la température de fusion est une fonction croissante de la pression. Pour la glace, au contraire, elle décroît lorsqu'on augmente la pression : ce phénomène permet d'expliquer la marche des glaciers.
4. Fusion d'un mélange
La température de fusion d'un mélange dépend de sa composition (→ cryoscopie). Le liquide et le solide qui coexistent à une température donnée n'ont pas la même composition; ainsi, la composition du solide varie pendant la fusion et donc aussi la température. On peut purifier un solide en procédant à une fusion partielle du mélange solide : le principe est le même que celui de la distillation.
CHIMIE
1. Zone de fusion des polymères
Les polymères semi-cristallins subissent, lorsqu'ils sont soumis à une température croissante, une transformation solide-liquide rappelant la fusion des cristaux de petites molécules. Cette transformation se manifeste en particulier par une brusque variation du volume massique. Elle se produit sur un intervalle de température dont la largeur peut être inférieure à un degré ou atteindre une dizaine de degrés; cet intervalle est dit « zone de fusion ».
2. Température de fusion des polymères
On définit en général la limite supérieure de la zone de fusion comme la température de fusion Tf. Tf dépend des facteurs suivants :
1) la longueur des chaînes et par conséquent la masse molaire : la température de fusion d'un polymère croît avec sa masse molaire, mais prend rapidement une valeur asymptotique ;
2) la rigidité des chaînes : Tf est d'autant plus élevé que les chaînes sont plus rigides ;
3) l'existence de liaisons intermoléculaires dites « secondaires », telles que les liaisons hydrogène ; ces liaisons peuvent être suffisamment fortes pour empêcher la fusion du produit (cellulose).
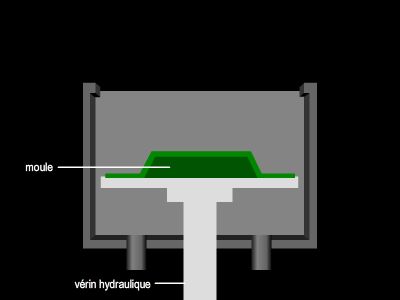
Lorsque les liaisons entre chaînes sont covalentes, la fusion n'est plus possible ; c'est le cas pour la plupart des phénoplastes, des aminoplastes, etc. De tels matériaux sont dits thermodurcissables, par opposition à ceux qui peuvent être fluidifiés par élévation de température et que l'on nomme thermoplastiques.
4) la disposition relative des macromolécules dans la matière : toutes choses égales par ailleurs, plus la disposition des chaînes est régulière, plus la température de fusion est élevée. Cela revient à dire que la température de fusion d'un polymère augmente avec son degré de cristallinité.
Cette propriété explique qu'un polyéthylène dit « haute densité », à degré de cristallinité élevé, puisse fondre à 140 °C, alors qu'un polyéthylène « basse densité », à degré de cristallinité inférieure, fond entre 110 et 115 °C.
À titre d'exemple, quelques points de fusion de polymères sont donnés ci-après :
• polytéréphtalate d'éthylène glycol (Tergal), 290-295 °C ;
• polyhexaméthylène adipamide (Nylon), 265 °C ;
• polyundécanamide (Rilsan), 185 °C.
Cependant, dans beaucoup de cas, la température de ramollissement d'un polymère dépend de son mode de préparation et des traitements qu'il a subis. Ainsi, un polystyrène peut, selon son origine, se ramollir entre 120 et 180 °C et même se déformer dès 70 °C. D'une façon générale, les copolymères statistiques fondent à une température inférieure à celle des homopolymères correspondants.
GÉOLOGIE

Une roche composée d'un assemblage de minéraux, chacun d'eux ayant son propre point de fusion, ne fond pas en bloc à une température donnée. La fusion débute lorsque la température du solidus est atteinte et se poursuit de façon non linéaire au fur et à mesure que la température augmente. La fusion partielle du manteau supérieur est à l'origine de la plus grande partie du magmatisme.
L'action soit mécanique, soit physique de la chaleur sur les surfaces des cristaux n'est pas la même en tous leurs points. Cette influence paraît s'étendre jusqu'aux actions chimiques elles-mêmes et se manifeste surtout lorsque ces actions s'exercent lentement et avec une faible intensité. La fusibilité par la flamme du chalumeau éprouve des variations sensibles dans quelques minéraux cristallisés, suivant la direction que l'on donne au dard de la flamme. Le gypse laminaire, par exemple, attaqué sur le plat de ses lames, se calcine sans fondre ; attaqué par la tranche, il subit une fusion préalable et se calcine ensuite.




![Diagramme de phases [4] Diagramme de phases [4]](/encyclopedie/data/vignettes/1003577-Diagramme_de_phases__4.jpg)