iode 131
Isotope radioactif de l’iode, noté 131 I, dont le nombre de masse est égal à 131.
L'iode 131 est un radio-isotope particulièrement redouté lorsqu’il est relâché par accident dans l’environnement, car il se concentre dans la thyroïde dont il peut perturber le fonctionnement.
1. Origines
L’iode 131 n’existe pas à l’état naturel. Toutefois, de l’iode 131 est produit naturellement lors des rares fissions spontanées de l’uranium naturel (→ radioactivité).
En revanche, de grandes quantités de ce radio-isotope sont produites par fission (uranium et plutonium) dans les réacteurs nucléaires. L’iode 131 est donc un déchet radioactif, classé parmi ceux de courte durée de vie du fait de sa période radioactive de 8,02 jours. Il est ainsi totalement éliminé par décroissance radioactive bien avant le démarrage de la phase de retraitement du combustible.
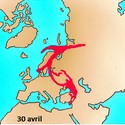
De grandes quantités d’iode 131 ont également été produites lors des nombreux essais nucléaires atmosphériques réalisés entre les années 1940 et 1990. Mais en raison de sa rapide décroissance radioactive, ces masses d’iode 131 ont depuis longtemps disparu.
Par ailleurs, à l’instar du césium 137, l’iode 131 est également l’une des principales sources de contamination radioactive lors des accidents de réacteurs nucléaires, dont les plus connus sont ceux des centrales de Three Miles Island (États-Unis) en 1979, de Tchernobyl (Ukraine) en 1986 et de Fukushima (Japon) en 2011.
2. Propriétés
Comme tous les isotopes de l’iode (qui compte 37 radio-isotopes au total), le noyau de l’iode 131 comporte 53 protons, mais il se distingue par son nombre de neutrons égal à 78. Son spin est de 7/2 et sa masse atomique est d’environ 130,906 (→ atome).
L’iode 131 se désintègre en xénon 131 (nucléide stable) selon le mode de désintégration β– (transmutation d’un neutron en proton) en émettant des rayons bêta (des électrons) et des rayons gamma de haute énergie (énergie de désintégration égale à 0,971 MeV).
C’est un isotope radioactif dont la durée de vie est considérée comme relativement courte. Sa période radioactive, ou temps de demi-vie (c’est-à-dire le temps au bout duquel la moitié des noyaux radioactifs, initialement présents, se sont désintégrés) est de 8,02 jours.
3. Toxicité
Du point de vue radiotoxicologique, l’iode 131 est un isotope à haut risque en raison de sa grande mobilité dans l’environnement, de sa bonne assimilation dans l’organisme et de son accumulation dans la thyroïde.
3.1. Effets de l’iode 131 sur la santé

La toxicité radioactive de l’iode 131 est mesurée par une quantité appelée « facteur de dose par ingestion », dont l’unité est le sievert par becquerel (Sv/Bq). Cette radiotoxicité varie considérablement avec l’âge de la personne exposée. En effet, l’iode se fixe sur la thyroïde qui joue notamment un rôle essentiel dans la croissance. C’est pourquoi les nourrissons et les enfants sont beaucoup plus sensibles que les adultes à l’ingestion d’iode radioactif.
On peut toutefois se prémunir d’une contamination à l’iode 131 en absorbant de l'iode non radioactif (généralement sous la forme de pastilles d'iodure de potassium KI), ce qui a pour effet de saturer la glande thyroïde. Mais il est inutile et dangereux de prendre systématiquement de l'iode à titre préventif. Le plus simple est de suivre les recommandations des pouvoirs publics, afin de prendre la bonne dose au bon moment.
Une fois fixé sur la thyroïde, la période biologique de l’iode 131 (c’est-à-dire le temps au bout duquel la moitié de l’iode 131 concentré dans la thyroïde est rejetée à l’extérieur de la glande) est d’environ 80 jours.
Pour en savoir plus, voir l'article irradiation.
3.2. Effets de l’iode 131 sur l’environnement
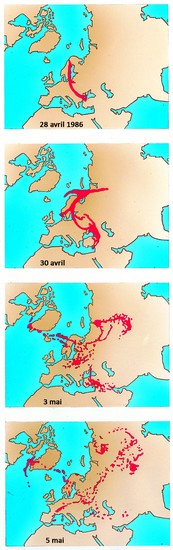
Dans l’environnement, l’iode 131 suit les processus de transfert habituels : dispersion aérienne, dépôt et captation par les végétaux, absorption par les racines, ingestion par l’animal.
Lors d’un accident nucléaire, la teneur en iode 131 est hautement surveillée dans la chaîne alimentaire durant plusieurs semaines. Les contrôles de radioactivité concernent principalement l’eau, le lait et les légumes à grandes feuilles comme les épinards et les laitues. Toutefois, du fait de sa courte période radioactive, la quantité d’iode 131 est divisée par deux tous les 8 jours, et est ainsi rapidement éliminée.
Différentes techniques sont utilisées pour la mesure de l’iode 131, notamment des méthodes de comptage par scintillation liquide et de spectrométrie gamma.
4. Utilisations diagnostique et thérapeutique
À faible dose, l’iode 131 est utilisé comme traceur pour des diagnostics en raison de ses rayons gamma. À l’aide de gamma-caméras, il est facile de suivre le devenir de ces radio-isotopes à travers l’organisme. L’iode se fixant sélectivement sur la thyroïde, cette technique d’imagerie (scintigraphie) est particulièrement intéressante puisqu’elle permet d’observer l’activité de la thyroïde et la présence d’éventuelles anomalies comme les nodules chauds ou froids. Toutefois, l’iode 131 est de plus en plus remplacé pour ces scintigraphies par un autre radio-isotope de l’iode, l’iode 123, également émetteur gamma et dont la période est plus courte (13,3 heures).
À plus forte dose, l’iode 131 est aussi utilisé pour les radiothérapies des cancers de la thyroïde. En effet, les rayons bêta émis par l’iode 131 permettent de détruire les cellules qui l’ont fixé. De plus, les rayons bêta ayant un faible parcours, l’irradiation est avantageusement limitée à la zone nécessaire à traiter. Ce traitement permet de réduire l’activité de la glande thyroïde ou de ses nodules en cas d’hyperthyroïdie, de compléter une ablation chirurgicale de la glande dans le cas d’un cancer ou encore de dépister l’apparition de métastases d’un cancer thyroïdien. Le traitement par des molécules marquées à l’iode 131 est en outre indiqué pour détruire ou réduire le volume de certaines tumeurs surrénaliennes ou hépatiques.
L’administration des différents isotopes d’iode radioactif se fait sous la forme d’iodures de sodium (NaI) ou de potassium (KI), ou encore d’iodate de potassium (KIO3).