uranium
(de urane)
Métal lourd, radioactif. (Élément chimique de symbole U.)
- Numéro atomique : 92
- Masse atomique : 238,03
- Masse volumique : 19,07 g/cm3
- Température de fusion : 1 132 °C
Introduction
Aujourd'hui, en France, l'essentiel de l'électricité consommée est d'origine nucléaire. Ce sont des réactions de fission de noyaux d'uranium 235 qui fournissent l'énergie nécessaire à la production de cette électricité.
L'essentiel de l'uranium extrait est destiné à la fabrication du combustible nucléaire (en 2002, la production mondiale s'élevait à 37,04 milliers de tonnes d'uranium métallique, les principaux pays producteurs étant le Canada, le Niger, la Russie, le Kazakhstan et la Namibie).
Historique de la découverte de l’uranium
L'oxyde d'uranium, l'urane (UO2), fut découvert, en 1789, par l'Allemand Martin Heinrich Klaproth. En analysant un minerai originaire de Saxe, la pechblende, ce chimiste met en évidence la présence d'une substance inconnue qui se comporte comme un métal et qu'il baptise uranium, d'après le nom de la planète Uranus, observée pour la première fois huit ans plus tôt par l'astronome anglais William Herschel.
Mais c'est Eugène Melchior Peligot qui en 1841 réussit à purifier et à obtenir un échantillon d'uranium métallique. En 1896, Henri Becquerel découvre que des sels d'uranium sont capables de produire un rayonnement : la radioactivité est née. L'analyse de la pechblende conduit les Français Pierre et Marie Curie à la découverte du polonium et du radium. En 1938, les physiciens allemands Otto Hahn et Fritz Strassmann analysent les propriétés de fission de certains noyaux d'uranium ayant été bombardés par des neutrons ; les recherches les plus importantes sur cet élément chimique débutent alors. Cette dernière découverte, ainsi que les travaux des physiciens Enrico Fermi, Leo Szilard, Carl David Anderson, Frédéric et Irène Joliot-Curie et d'autres permettent la réalisation, dès 1942, de la première réaction nucléaire en chaîne.
Depuis, les explosions des bombes atomiques sur les villes d'Hiroshima et de Nagasaki lors de la Seconde Guerre mondiale et l'accident de la centrale nucléaire de Tchernobyl, ont montré la puissance et les dangers de cette source d'énergie.
La géochimie de l'uranium
Dans la lithosphère, la teneur en uranium est de l'ordre de 3 à 4 ppm : c'est un élément chimique relativement rare.
On le trouve essentiellement sous forme d'inclusions dans certains minéraux. Les réserves sont situées principalement en Australie, aux États-Unis, au Canada et en Afrique du Sud. La prospection de l'uranium se fait essentiellement par radiométrie ou par prospection géochimique.
L'uranium naturel est un mélange de trois isotopes radioactifs dont les nombres de masse, les périodes radioactives (ou temps de demi-vie, c’est-à-dire le temps au bout duquel la moitié des noyaux radioactifs se sont désintégrés) et les proportions dans l’élément naturel sont les suivants :
U 238 : période radioactive de 4,46.109 ans, constituant 99,27 % de l’uranium naturel ;
U 235 : période radioactive de 7,04.108 ans, constituant 0,72 % de l’uranium naturel ;
U 234 : période radioactive de 2,45.105 ans, constituant 0,006 % de l’uranium naturel.
L'isotope 235 est le seul radionucléide naturel qui soit fissile.
Les propriétés physico-chimiques de l’uranium
L'uranium métallique
D'aspect, l'uranium métallique ressemble beaucoup au nickel (même couleur, textures similaires).
Les propriétés mécaniques de l'uranium métallique dépendent de son mode de fabrication. Cependant, il est généralement malléable et ductile. C'est un métal très réactif, très inflammable et oxydable. Il peut se combiner avec d'autres éléments chimiques (chlore, soufre, azote, carbone).
Les composés de l'uranium
Les oxydes d’uranium
Les oxydes de l'uranium les plus courants sont l'oxyde uraneux UO2, l'oxyde salin U3O8 et l'anhydride uranique UO3.
L'oxyde uraneux (UO2) est stable thermiquement. Il ne réagit pas avec l'eau, et il est donc utilisé en priorité pour l'industrie nucléaire.
L'anhydride uranique (UO3), lui, est plus réactif et il est utilisé en tant qu'intermédiaire. Il est obtenu par calcination de l'oxyde uraneux.
L'oxyde salin (U3O8) se trouve à l'état naturel dans la pechblende. C'est une association de UO2 et de UO3 et par conséquent il possède les propriétés décrites ci-dessus des deux autres oxydes.
Les halogénures d’uranium
Les principaux halogénures d’uranium sont le tétrafluorure d'uranium UF4 et l'hexafluorure d'uranium UF6.
L'hexafluorure d'uranium (UF6) est volatil, incolore et se sublime aisément. Il est utilisé pour réaliser des opérations d'enrichissement isotopique.
Le tétrafluorure d'uranium (UF4) est lui un excellent intermédiaire de synthèse.
Complexes, sels et hydroxydes d’uranium
Les complexes de l'uranium sont très nombreux et sont d'autant plus stables que leurs ligands sont basiques.
Les plus rencontrés sont obtenus à partir des ions UO22+, nitrates NO3− et sulfates SO42− et sont très stables.
En milieu basique, les ions U4+ et UO22+ sont facilement hydrolysés et conduisent à la formation de précipités et d'hydroxydes solubles.
Le minerai naturel (pechblende ou uranite) doit subir différents traitements mécaniques et chimiques sur le site même de l'exploitation avant d'être transporté vers les centrales nucléaires où il sera soumis aux derniers traitements en vue de l'obtention du combustible nucléaire.
Traitement des minerais d’uranium
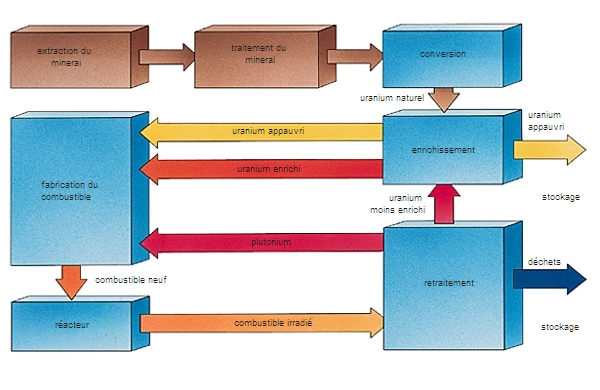
Les minerais d’uranium présents dans la nature ne sont donc pas directement exploitables. Il faut les concentrer avant de les utiliser, ce qui est réalisable en solution. Les différentes opérations ont lieu sur le site même de l'exploitation. La métallurgie de l'uranium comporte plusieurs phases distinctes.
Obtention du concentré uranifère
Traitements mécaniques
Le minerai d’uranium extrait d'un site d'exploitation est concassé et broyé dans un premier temps de manière à obtenir une poudre fine susceptible de se solubiliser facilement.
Lixiviation acide
Cette poudre doit être mise en solution avant la concentration. Aujourd'hui, la lixiviation acide est le procédé le plus employé. On fait agir sur le minerai une solution d'acide sulfurique, ce qui a pour effet de solubiliser les oxydes sous forme de sulfates d'uranyle (sels de sulfate et d'uranium). À cette étape du traitement, les sels d'uranium sont encore mélangés avec d'autres composés chimiques ne contenant pas d'uranium, ce qui rend nécessaire une étape de séparation.
Séparation
Pour cette opération, on utilise une résine échangeuse d'ions qui retient les sels d'uranium et laisse passer les impuretés. À ce stade, les solutions obtenues contiennent 20 g d'élément uranium par litre (sous forme du sel UO2(SO4)34−), ce qui est encore insuffisant. Une autre étape de concentration est donc nécessaire.
Concentration
Dans la solution obtenue après séparation, l'ion contenant l'élément uranium est l'ion uranyle UO22+ qui précipite facilement en présence d'une base forte ou d'un oxyde basique.
On met à profit cette propriété dans l'opération de concentration puisque l'on y fait précipiter sélectivement l'ion UO22+ en présence de MgO afin d'obtenir un solide à base de MgUO4 dans lequel la teneur en uranium atteint 70 %.
Le composé ainsi obtenu peut être transporté loin du site d'exploitation pour y subir les derniers traitements nécessaires à la fabrication du combustible, notamment, l'opération de purification.
La purification
Afin d'améliorer la qualité du composé obtenu, on le soumet à l'action de l'acide nitrique et de l'ammoniac. On obtient ainsi le diuranate d'ammonium ((NH4)2U2O7), ou concentré uranifère, qui possède une pureté nucléaire mais qui est malheureusement très peu riche en isotope 235 de l'uranium (seul isotope fissible et donc utilisable dans un réacteur nucléaire).
Il est donc nécessaire d'enrichir ce composé en isotope 235.
L'enrichissement isotopique
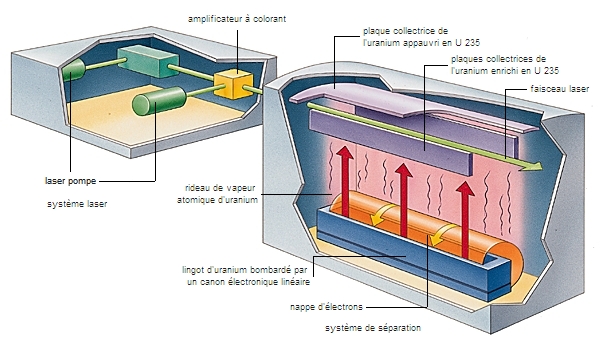
Le diuranate d'ammonium est tout d'abord calciné, ce qui conduit à la formation de UO3.
UO3 est ensuite réduit en UO2, lequel est soumis à l'action de fluorure d'hydrogène gazeux (HF). On obtient ainsi le tétrafluorure d’uranium solide UF4 qui, en présence de difluor gazeux, conduit à la formation de l’hexafluorure d’uranium UF6.
Ce dernier est ensuite soumis à un procédé de diffusion gazeuse qui a pour effet d'enrichir le composé en isotope 235.
Fabrication du combustible nucléaire
Pour être utilisable dans les réacteurs nucléaires, l'élément combustible doit être constitué de l'uranium de qualité nucléaire enrichi (sous forme métallique, ou sous forme d'alliage ou d'oxyde) et d'une gaine (en acier, en magnésium, en zirconium…).
Ces opérations de fabrication sont réalisées à proximité des réacteurs et on fabrique ainsi des éléments combustibles dont la forme dépend du type de réacteur.
Retraitement des déchets radioactifs
Lorsque 1 000 kg de combustible pénètrent à l'intérieur d'un réacteur nucléaire, ils génèrent à la sortie de ce réacteur plus de 950 kg de déchets dont beaucoup sont radioactifs. La plupart d'entre eux sont retraités afin d'être réutilisés. Seulement, lorsque le retraitement n'est pas possible ou trop peu rentable, se pose le problème du stockage de ces déchets, en particulier ceux à vie longue (plusieurs milliers d’années).
GÉOGRAPHIE
La production mondiale annuelle (en métal contenu) avoisine 35 000 tonnes. Le Canada occupe le premier rang mondial (12 000 tonnes), loin devant l'Australie (5 000 tonnes), le Niger (3 000 tonnes), le Kazakhstan, l'Ouzbékistan et la Russie (1 500 à 3 000 tonnes chacun). La France est le deuxième producteur européen (700 tonnes), derrière l'Ukraine. Les réserves sont estimées à plus de 1,5 million de tonnes (dont environ 25 000 tonnes en France).
GÉOLOGIE
L'uranium se concentre dans le liquide résiduel au cours de la cristallisation magmatique et on le trouve dans les roches très différenciées. Sa distribution peut être modifiée par les phénomènes hydrothermaux ou l'altération. Les gisements d'uranium sont généralement détectés par radiométrie. La désintégration des isotopes de l'uranium est utilisée dans la datation des roches. (→ géochronologie.)