acide tartrique

Acide CO2H―(CHOH)2―CO2H, découvert en 1769 par Scheele dans le tartre.

CHIMIE
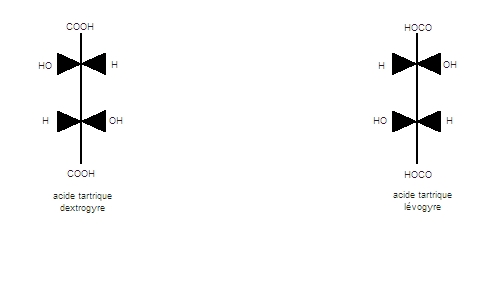
L'acide tartrique comporte deux atomes de carbone asymétriques qui ont le même environnement. L'acide tartrique dextrogyre, ou acide L-tartrique, est celui dont le sel monopotassique est le tartre naturel ; il a la configuration S, S. On l'emploie comme rongeant en teinturerie. Par chauffage avec l'eau sous pression ou en présence de soude, il se transforme en acide racémique et en acide mésotartrique. L'acide racémique, ou paratartrique, est le mélange équimoléculaire des deux énantiomères : acide L-tartrique et acide D-tartrique ; on le rencontre parfois au cours de la vinification, mais c'est très probablement un artefact. Pasteur a découvert l'acide lévogyre ou D-tartrique lors de la résolution de l'acide racémique. L'acide mésotartrique possède un plan de symétrie et ne peut donc être résolu en énantiomères.




