calorimétrie
Mesure des quantités de chaleur dans les divers phénomènes où celle-ci est mise en jeu.
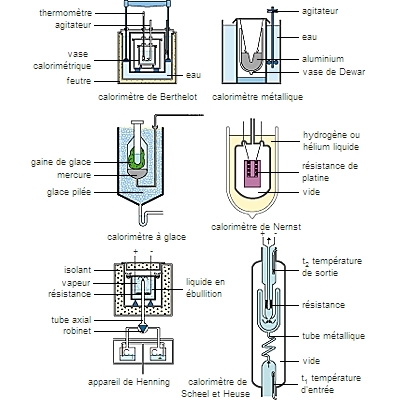
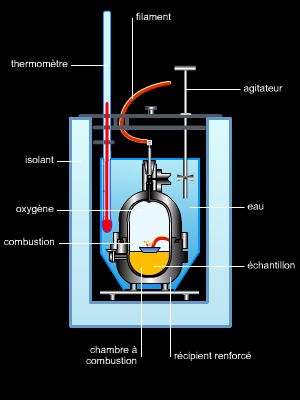
Les principes de la calorimétrie (principe des transformations inverses et principe de l'égalité des échanges de chaleur) s'appliquent à des systèmes isolés thermiquement. Pour limiter les échanges thermiques parasites entre le système proprement dit et l'environnement, par rayonnement, conduction et convection, on utilise des parois réfléchissantes et des supports isolants ; si possible, on opère dans le vide et on maintient l'enceinte extérieure à la même température que le système. La méthode calorimétrique utilisée par le calorimètre de Berthelot ou le calorimètre métallique consiste à mesurer la variation de température subie par un liquide (eau, huile) ou un métal (cuivre, aluminium), mis en contact avec le système à étudier, variation qui est proportionnelle à la quantité de chaleur cherchée. Avec le calorimètre à glace, on mesure la masse (ou le volume) de glace ayant fondu au contact du système, à température constante. Les méthodes calorimétriques électriques sont les plus employées. Elles consistent à réaliser à l'aide d'une énergie électrique la même transformation que celle produite par la quantité de chaleur à mesurer. Pour cela, on place, dans un fluide ou un solide, une résistance chauffante. L'énergie électrique dépensée pendant un temps donné est égale à la quantité de chaleur à déterminer. On mesure ainsi les chaleurs massiques des solides et des fluides et les chaleurs latentes de vaporisation des liquides. Pour les mesures microcalorimétriques (chaleurs de réaction en chimie organique, phénomènes thermiques en biologie, etc.), on utilise des calorimètres électriques à effet Peltier.