diènes et polyènes
Les diènes sont des hydrocarbures renfermant deux liaisons éthyléniques ; les polyènes en comportent un plus grand nombre.
Les diènes se subdivisent en diènes cumulés 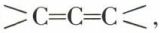 diènes conjugués
diènes conjugués 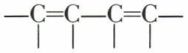 et diènes plus éloignés.
et diènes plus éloignés.
Le règne végétal nous fournit quelques diènes, le plus souvent conjugués et appartenant à la série terpénique, ainsi que plusieurs polyènes indéfinis non conjugués (caoutchouc naturel).
Nomenclature
Les diènes portent le nom de l’hydrocarbure saturé correspondant dont l’e final fait place à la désinence diène avec, si besoin est, des numéros d’ordre ; pour les polyènes, on emploie les désinences triène, tétraène, etc. :
CH2=C(CH3)—CH=CH2 méthyl-2 butadiène-1-3 (isoprène),
CH2=CH—CH=CH—CH=CH2 hexatriène-1-3-5.
État naturel et préparations
Le butadiène-1-3 existe, à faible concentration, dans le gaz d’éclairage ; l’isoprène se forme par pyrogénation des terpènes ou du caoutchouc naturel.
Mais la plupart des diènes et polyènes sont synthétiques, et leurs préparations varient avec la distance des liaisons éthyléniques.
Les diènes n, n + 1 ou diènes cumulés sont avantageusement préparés grâce à une transposition partielle :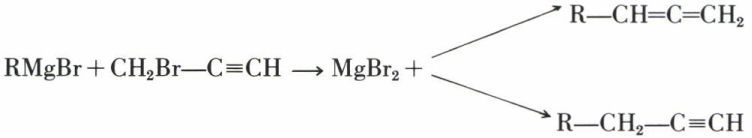
Ces deux carbures doivent être séparés.
Les diènes n, n + 2 (diènes conjugués) sont industriellement préparés par déshydrogénation des alcanes ou des alcènes ; la pyrogénation du butane ou du butène de craquage est la source la plus économique de butadiène-1-3.
Mais on peut aussi déshydrater divers alcools, (CH3)2CHOH—CH=CH2, CH3—CH=CH—CH2OH, et divers glycols, CH3—CHOH—CH2—CH2OH, (CH3)2COH—COH(CH3)2, ou des éthers-oxydes cycliques (tétrahydrofuranne).
Ces matières premières sont les intermédiaires dans plusieurs des préparations industrielles.
Les diènes n, n + 3 sont peu accessibles, et les diènes n, n + 4 résultent de réactions de Wurtz :
2 CH=CH—CH2Br + 2 Na → 2 NaBr + CH2=CH—CH2—CH2—CH=CH2.
Propriétés physiques
Les diènes cumulés et conjugués présentent des anomalies. Par exemple, en infrarouge, la bande d’absorption des diènes cumulés (1 956 cm–1) est très éloignée de celle des alcènes (1 640-1 680) ; les diènes conjugués voient au contraire la fréquence éthylénique abaissée. Ces hydrocarbures sont très réfringents et dispersifs.
Propriétés chimiques
Les diènes cumulés sont d’un intérêt réduit ; signalons seulement deux isomérisations :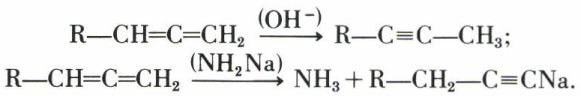
Les diènes conjugués sont fortement désaturés, ils se comportent deux fois comme tels dans les réactions d’addition valables pour les monoéthyléniques ; mais la première addition peut se faire de deux façons :
CH2=CH—CH=CH2 + X2 → CH2X—CHX—CH=CH2 (addition 1-2) ;
CH2=CH—CH=CH2 + X2 → CH2X—CH=CH—CH2X (addition 1-4).
Selon la nature de X et selon les substituants introduits dans le butadiène-1-3, l’une des additions est prépondérante.
Par contre, les additions, qui n’ont pas lieu sur la liaison éthylénique isolée, se font exclusivement en 1-4 : la plus caractéristique est la « synthèse diénique » (addition du diène sur la liaison multiple activée d’un accepteur appelé philodiène).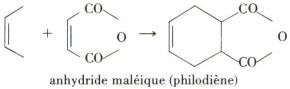
L’intérêt pratique, presque exclusif, des diènes conjugués est la polymérisation indéfinie (sodium, peroxydes) :
nCH2=CH—CH=CH2 → —CH=CH—CH2—CH2—CH2—CH=CH—CH2—CH2...
(buna)
Ces polymères constituent les caoutchoucs synthétiques (élastomères), mais la copolymérisation avec d’autres composés non saturés — styrolène, nitrile acrylique, etc. — conduit à des élastomères de propriétés particulières (caoutchoucs GRS, GRN, etc.).
Les diènes éloignés ne présentent aucune anomalie physique ni chimique.
Les polyènes entièrement conjugués sont au contraire caractérisés par des anomalies physiques accentuées : 5 doubles liaisons conjuguées amènent une légère coloration jaune verdâtre ; 11 doubles liaisons (cas des carotènes) déplacent le spectre d’absorption UV assez loin dans le visible (coloration orangée).
Les polyènes indéfinis non conjugués ont pour prototype le caoutchouc naturel : chaîne « polyprénique » :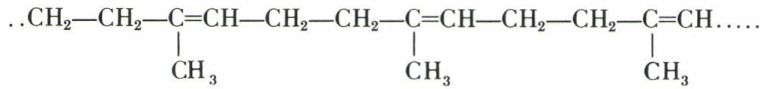
La pyrogénation conduit à l’isoprène, l’ozonolyse à l’aldéhyde lévulique CH3—CO—CH3—CH3—CHO, ce qui établit la constitution.
Otto Diels
Chimiste allemand (Hambourg 1876 - Kiel 1954). Il est, avec son élève Kurt Alder (1902-1958), l’auteur, en 1928, de la « synthèse diénique », qui a permis l’obtention du camphre, de la vitamine D et de la cortisone. Tous deux ont reçu le prix Nobel de chimie en 1950.
C. P.
Diesel (moteur)
Moteur à combustion interne utilisant des combustibles liquides lourds qui, injectés dans une masse d’air fortement comprimée, s’enflamment spontanément.
Comparaison avec le moteur à essence
Le moteur à huile lourde, improprement appelé du nom de l’inventeur d’un cycle de fonctionnement inapplicable à un modèle à grande vitesse de régime, ressemble au moteur à essence, dont il adopte la structure générale. Cependant, ce moteur ne comporte ni appareil d’allumage ni carburateur, l’inflammation du mélange étant obtenue par simple injection du carburant, qui, pulvérisé dans un milieu gazeux fortement comprimé, est ainsi porté à une température très élevée. Le rapport volumétrique de compression, qui n’est que de 7 ou 8 à 1 pour un moteur à essence classique, atteint, ici, des valeurs se situant entre 12 et 16 à 1, ce qui explique l’excellent rendement thermique du moteur à huile lourde. On évite l’apparition prématurée du phénomène de détonation uniquement par la compression de l’air seul, mais il existe toujours un risque de production de pression explosive trop élevée, provoquée soit par l’utilisation d’une avance à l’injection trop importante, soit par la combustion additionnelle de l’huile de graissage, admise à l’intérieur des cylindres. Pour en tenir compte, on est tenté d’accroître la résistance de la structure en augmentant le poids. À la rigueur, l’importance est minime s’il ne s’agit que d’un emploi industriel, à poste fixe ou d’une utilisation marine. Pour le moteur d’automobile, cette pratique va à l’encontre des recherches actuelles, où l’on s’efforce d’améliorer la puissance massique en allégeant l’ensemble, dans la mesure où le respect des normes de la sécurité le permet. De ce fait, le rendement mécanique du moteur à huile lourde est toujours inférieur à celui du moteur à essence.




